El Reglamento de productos sanitarios (UE) 2017/745, conocido como MDR (Medical Device Regulation), ha transformado profundamente la regulación de los productos sanitarios en Europa desde su entrada en vigor completa el 26 de mayo de 2024. Este marco legal busca garantizar que todos los dispositivos médicos disponibles en el mercado sean seguros, efectivos y cumplan con los más altos estándares de calidad.
En CINCOS, además de ofrecerte la mejor máquina de presoterapia para tu centro de entre todo nuestro catálogo, también te queremos informar de que las normativas vigentes son esenciales para asegurar la seguridad y eficacia de los equipos que utilizas diariamente. Por eso, te desglosamos los aspectos clave del reglamento de productos sanitarios vigente y sus implicaciones actuales para que estés al día.
¿Qué son los productos sanitarios?
Un producto sanitario se define como cualquier instrumento, dispositivo, equipo, software, material u otro artículo destinado por su fabricante a ser utilizado en humanos con fines específicos relacionados con:
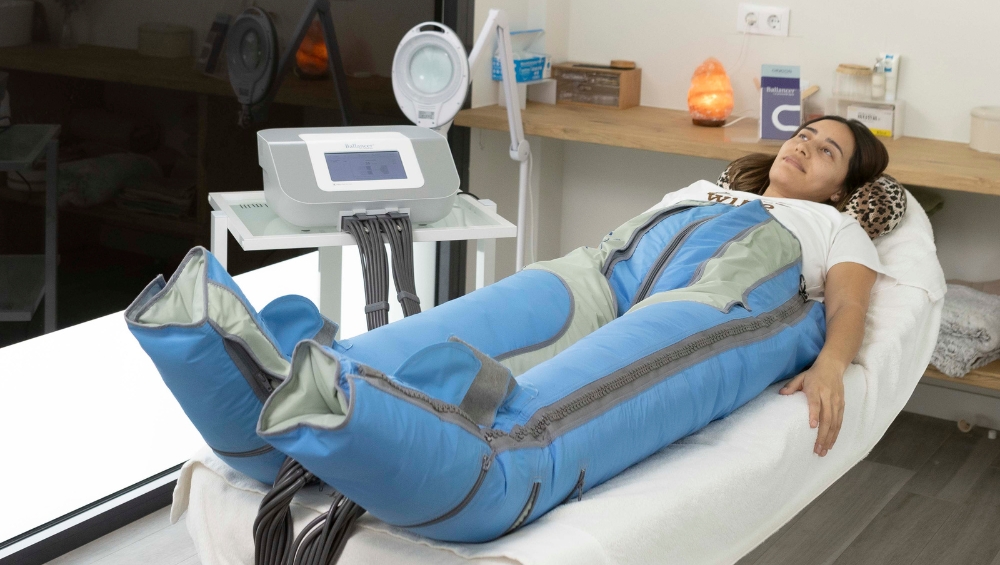
Este amplio concepto de “productos sanitarios” incluye desde jeringas y vendajes hasta sofisticados equipos médicos, como las máquinas de presoterapia, diseñadas para mejorar la circulación y reducir edemas.
Principales novedades del Reglamento MDR en 2025
Desde su entrada en vigor total en 2024, el MDR ha introducido cambios significativos que afectan tanto a grandes fabricantes como a pequeñas empresas. A continuación, destacamos las principales innovaciones:
¿Cómo nos afecta el Reglamento MDR 2017/745? Principales novedades en 2025
El Reglamento (UE) 2017/745 ha introducido cambios significativos en la regulación de los productos sanitarios desde su publicación en 2017 y su entrada en vigor completa en mayo de 2024. Estas novedades tienen un impacto directo tanto en fabricantes como en distribuidores, importadores y profesionales del sector. Las principales innovaciones que debemos tener más en cuenta, son:
Impacto del Reglamento MDR en PYMES y startups
El cumplimiento del Reglamento MDR 2017/745 puede representar a veces un desafío para las pequeñas y medianas empresas (PYMES) y startups que se dediquen al sector de productos sanitarios. Estas empresas suelen operar con recursos limitados, lo que complica su adaptación a los nuevos requisitos regulatorios más estrictos. Sin embargo, tanto a nivel nacional como europeo se han desarrollado programas de apoyo específicos para facilitar este proceso en la medida de lo posible.
Programas de apoyo para PYMES y startups
Para ayudar a estas empresas a cumplir con el reglamento de productos sanitarios MDR, se han implementado diferentes iniciativas que incluyen:
En CINCOS, entendemos perfectamente estos cambios y nos comprometemos a cumplir con todas las normativas aplicables, garantizando que todos nuestros equipos sean referentes en calidad y seguridad. Nuestro objetivo no solo es adaptarnos a los cambios regulatorios, sino también liderar el camino hacia un futuro más seguro y eficiente en el sector de los productos sanitarios.
A través de nuestra experiencia y dedicación, trabajamos para ofrecer tecnologías innovadoras que cumplan con las exigencias del MDR, al tiempo que apoyamos a otras empresas del sector en su proceso de adaptación.
Productos sanitarios sin finalidad médica
El Reglamento de productos sanitarios MDR 2017/745 no solo regula dispositivos médicos tradicionales, sino también ciertos productos que, aunque no tienen una finalidad médica explícita, interactúan directamente con el cuerpo humano y requieren un control similar debido a su potencial impacto en la salud de las personas.
Estos productos, definidos en el artículo 1, apartado 2, del reglamento de productos sanitarios abarcan diversas categorías:
Clasificación de los productos sanitarios
Los productos sanitarios se clasifican en función de su grado de riesgo potencial para la salud del usuario. Esta clasificación permite establecer requisitos regulatorios proporcionales al nivel de riesgo, garantizando una evaluación adecuada de cada dispositivo. Según el Reglamento MDR 2017/745, existen cuatro clases principales:
Características por cada clase
En resumen, a medida que aumenta la clase de riesgo, también lo hacen los requisitos regulatorios necesarios para obtener el marcado CE.
¿Cómo se determina la clase de riesgo?
La normativa europea evalúa el grado de riesgo de un producto sanitario considerando varios factores clave:
Adaptación a las nuevas exigencias del MDR
Desde la entrada en vigor completa del Reglamento MDR en mayo de 2024, todos los productos sanitarios deben cumplir con los nuevos criterios de clasificación y requisitos regulatorios. Esto implica:
Por ejemplo, muchas máquinas de presoterapia, que anteriormente podían clasificarse como Clase I , ahora pueden requerir una reevaluación debido a su uso prolongado y su interacción directa con la piel.
Tendencias tecnológicas en productos sanitarios
En 2025 debemos tener en cuenta que la digitalización y la inteligencia artificial (IA) están revolucionando el mundo, y también el sector de los productos sanitarios. Hoy en día, muchos dispositivos incorporan tecnología avanzada para mejorar su precisión y eficiencia.
Por ejemplo, las máquinas de presoterapia modernas cuentan con sensores inteligentes que ajustan automáticamente la presión según las necesidades del paciente.
Esta evolución tecnológica exige que los fabricantes estén constantemente actualizados en materia regulatoria, ya que los dispositivos digitales suelen requerir evaluaciones adicionales para garantizar su funcionamiento seguro.
El Reglamento MDR 2017/745 ha establecido un nuevo estándar para la industria de los productos sanitarios, priorizando la seguridad y el bienestar de los pacientes. En CINCOS, estamos comprometidos con cumplir estas exigencias y ofrecer a nuestros clientes soluciones de alta calidad que cumplen con todas las normativas vigentes.
Si deseas conocer más sobre cómo podemos ayudarte a equipar tu centro con tecnología avanzada y segura, no dudes en contactarnos sin compromiso.